Письмо Федеральной службы по надзору в сфере здравоохранения от 9 февраля 2016 г. N 01И-219/16 "Об отзыве деклараций о соответствии"
Федеральная служба по надзору в сфере здравоохранения сообщает о проведении АО "Астеллас Фарма" процедуры отзыва деклараций о соответствии на лекарственные препараты:
1. " таблетки, покрытые пленочной оболочкой 120 мг 8 шт., блистеры (14), пачки картонные" производства ЗАО "Р-ФАРМ", Россия/ЗАО "ОРТАТ", Россия:
таблетки, покрытые пленочной оболочкой 120 мг 8 шт., блистеры (14), пачки картонные" производства ЗАО "Р-ФАРМ", Россия/ЗАО "ОРТАТ", Россия:
- N РОСС RU.ФВ14.Д05144 от 19.12.2014 (серия 509122014);
- N РОСС RU.ФВ14.Д05777 от 28.01.2015 (серия 551122014);
- N РОСС RU.ФВ14.Д05855 от 30.01.2015 (серия 04012015);
- N РОСС RU.ФВ14.Д07434 от 15.04.2015 (серия 138032015);
- N РОСС RU.ФВ14.Д07260 от 07.04.2015 (серия 120032015).
2. " таблетки, покрытые пленочной оболочкой 120 мг 8 шт., блистеры (7), пачки картонные" производства "Астеллас Фарма Юроп Б.В.", Нидерланды/ЗАО "ОРТАТ", Россия:
таблетки, покрытые пленочной оболочкой 120 мг 8 шт., блистеры (7), пачки картонные" производства "Астеллас Фарма Юроп Б.В.", Нидерланды/ЗАО "ОРТАТ", Россия:
- N РОСС RU.ФВ14.Д06118 от 12.02.2015 (серия 39012015);
- N РОСС RU.ФВ14.Д07047 от 30.03.2015 (серия 110032015);
- N РОСС RU.ФВ14.Д07419 от 15.04.2015 (серия 145032015);
- N РОСС RU.ФВ14.Д07417 от 15.04.2015 (серия 143032015);
- N РОСС RU.МП25.Д24791 от 21.07.2015 (серия 316062015);
- N РОСС RU.МП25.Д22789 от 23.06.2015 (серия 270062015);
- N РОСС RU.ФВ14.Д07415 от 15.04.2015 (серия 140032015).
3. " таблетки, покрытые пленочной оболочкой 120 мг 8 шт., блистеры (7), пачки картонные" производства ЗАО "Р-ФАРМ", Россия/ЗАО "ОРТАТ", Россия:
таблетки, покрытые пленочной оболочкой 120 мг 8 шт., блистеры (7), пачки картонные" производства ЗАО "Р-ФАРМ", Россия/ЗАО "ОРТАТ", Россия:
- N РОСС RU.МП25.Д21904 от 08.06.2015 (серия 249052015).
4. "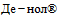 таблетки, покрытые пленочной оболочкой 120 мг 8 шт., блистеры (7), пачки картонные" производства ЗАО "Р-ФАРМ", Россия/ЗАО "ОРТАТ", Россия:
таблетки, покрытые пленочной оболочкой 120 мг 8 шт., блистеры (7), пачки картонные" производства ЗАО "Р-ФАРМ", Россия/ЗАО "ОРТАТ", Россия:
- N РОСС NL.ФМ09.Д59710 от 29.07.2013 (серия 13Е02/21).
О приостановлении реализации указанных серий лекарственных препаратов субъекты обращения лекарственных средств информированы письмами Росздравнадзора: от 15.07.2015 N 01И-1155/15, от 21.07.2015 N 01И-1174/15, от 18.08.2015 N 02И-1343/15, от 06.10.2015 N 01И-1634/15, от 13.10.2015 N 01И-1709/15, от 15.10.2015 N 01И-1730/15, от 22.10.2015 N 01И-1778/15, от 21.10.2015 N 01И-1768/15, от 18.11.2015 N 01И-1973/15, от 18.12.2015 N 02И-2212/15.
Росздравнадзор предлагает АО "Астеллас Фарма" предоставить сведения об изъятии из обращения данных серий лекарственных препаратов, выпущенных в гражданский оборот на основании указанных деклараций о соответствии.
Федеральная служба по надзору в сфере здравоохранения предлагает субъектам обращения лекарственных средств предоставить в территориальный орган Росздравнадзора сведения, подтверждающие изъятие из обращения указанных серий лекарственных препаратов, выпущенных в гражданский оборот на основании перечисленных деклараций о соответствии.
Территориальным органам Росздравнадзора обеспечить контроль за выявлением и изъятием вышеуказанных серий лекарственных препаратов, выпущенных в гражданский оборот на основании данных деклараций о соответствии. О проведенной работе информировать Росздравнадзор.
| М.А. Мурашко |
Обзор документа
АО "Астеллас Фарма" отзывает декларации о соответствии на лекарственный препарат "Де-нол" 120 мг производства ЗАО "Р-ФАРМ" Россия: N РОСС RU.ФВ14.Д05144 от 19.12.2014 (серия 509122014); N РОСС RU.ФВ14.Д05777 от 28.01.2015 (серия 551122014); N РОСС RU.ФВ14.Д05855 от 30.01.2015 (серия 04012015); N РОСС RU.ФВ14.Д07434 от 15.04.2015 (серия 138032015); N РОСС RU.ФВ14.Д07260 от 07.04.2015 (серия 120032015); N РОСС RU.МП25.Д21904 от 08.06.2015 (серия 249052015); N РОСС NL.ФМ09.Д59710 от 29.07.2013 (серия 13Е02/21).
Кроме того, отзываются декларации о соответствии на лекарственный препарат "Де-нол" 120 мг производства производства "Астеллас Фарма Юроп Б.В." (Нидерланды): N РОСС RU.ФВ14.Д06118 от 12.02.2015 (серия 39012015); N РОСС RU.ФВ14.Д07047 от 30.03.2015 (серия 110032015); N РОСС RU.ФВ14.Д07419 от 15.04.2015 (серия 145032015); N РОСС RU.ФВ14.Д07417 от 15.04.2015 (серия 143032015); N РОСС RU.МП25.Д24791 от 21.07.2015 (серия 316062015); N РОСС RU.МП25.Д22789 от 23.06.2015 (серия 270062015); N РОСС RU.ФВ14.Д07415 от 15.04.2015 (серия 140032015).
АО "Астеллас Фарма" следует предоставить сведения об изъятии из обращения данных серий лекарственных препаратов, сопровождающихся указанными декларациями о соответствии.



(1).jpg)


